導入
| コエンザイムA | |
|---|---|
 | |
| 一般的な | |
| IUPAC名 | |
| 同義語 | CoA または CoA-SH |
| CAS番号 | 85-61-0 |
| No.EINECS | 201-619-0 |
| ドラッグバンク | DB01992 |
| パブケム | 6816 3312 |
| 笑顔 | |
| インチチ | |
| 化学的性質 | |
| 生のフォーミュラ | C 21 H 36 N 7 W 16 P 3 S |
| モル質量 | 767.534 ± 0.031 g mol -1 |
| 生態毒性学 | |
| ログP | -5,340 |
コエンザイム A (CoA) は、多くの代謝経路 (クレブス回路、ベータ酸化) に関与するアシル基転移補酵素です。
これは、1951 年にドイツの生化学者フョードル ライネン (1964 年にノーベル賞を受賞) によって、酵母細胞からアセチル補酵素 A (「活性化酢酸」) の形で初めて単離されました。

構造
コエンザイム A は、ヌクレオチド、アデノシン二リン酸 (ADP)、ビタミン、ビタミン B5 (パントテン酸)、およびアミノ酸であるシステインの異なる要素で構成されており、わずかに修飾されて結合しています。
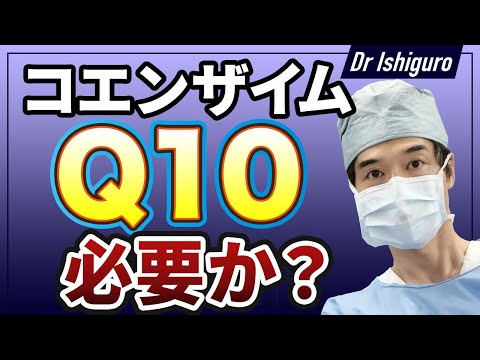
詳細には、コエンザイム A は次のもので構成されています。
その反応部分はチオエタノールアミンのチオール官能基 (-SH) (図 1) であり、HS-CoA (または CoA-SH) で表されることがよくあります。
カルボン酸との反応性
システアミンのチオール機能のおかげで、補酵素 A は、特定の化合物 (脂肪酸など) のカルボキシル官能基とカルボキシル CoA と呼ばれるチオエステルを形成することができます。このチオエステル結合は特にエネルギーが豊富です。
CoA-SH + R-COOH ⇒ CoA-S-CO-R ( + H 2 O )
したがって、コエンザイム A は脂肪の代謝に直接 (アシル CoA として) 関与し、炭水化物およびタンパク質の代謝には間接的に (アセチル CoA として) 関与します。
コエンザイムAは、パートナーと形成する高エネルギーのチオエステル結合を介してパートナーを「活性化」し、補酵素によって活性化されなければ参加しないであろう反応に参加できるようにするといわれています。
生合成
コエンザイムAは、パントテン酸(ビタミンB5)の共役塩基であるパントテネートから5段階で合成されます。
- パントテネートは、酵素パントテネートキナーゼ (PanK、CoaA、CoaX) によって 4′-ホスホパントテネートにリン酸化されます。
- 酵素ホスホパントテノイルシステイン合成酵素 (CoaB) によってシステイン分子が 4′-ホスホパントテネートに付加されて、4′-ホスホ-N-パントテノイルシステイン (PPC) が形成されます。
- PPCは、酵素ホスホパントテノイルシステインデカルボキシラーゼ(PPC-DC、CoaC)の作用により4′-ホスホパンテテインに脱炭酸されます。
- 4′-ホスホパンテテインは、 酵素ホスホパンテテイン アデニリルトランスフェラーゼ(CoaD) の作用によりアデニリル化され (アデノシン一リン酸の付加)、デホスホ CoA を形成します。
- 脱リン酸-CoA は、酵素脱リン酸コエンザイム A キナーゼ(CoaE) の作用による ATP との反応により、最終的にリン酸化されてコエンザイム A になります。
CoA ソース
ホルモン、キノコ、肉、卵黄。
