導入
| ベンゼンスルホン酸 | |||
|---|---|---|---|
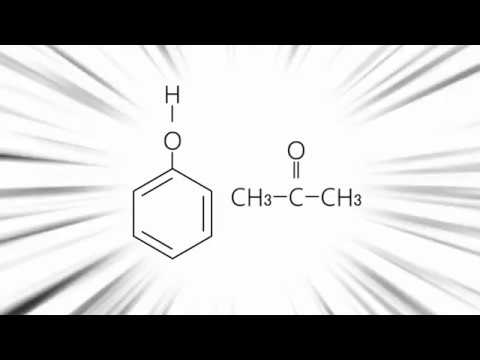 | |||
| 一般的な | |||
| IUPAC名 | |||
| CAS番号 | 98-11-3 | ||
| No.EINECS | 202-638-7 | ||
| パブケム | 7271 | ||
| 笑顔 | |||
| インチチ | |||
| 外観 | 灰色から黄色の単色 | ||
| 化学的性質 | |||
| 生のフォーミュラ | C6H6O3S | ||
| モル質量 | 158.175 ± 0.011 g mol -1 | ||
| pKa | 2,554 | ||
| 物性 | |||
| 融解温度 | 43 ℃ | ||
| 沸騰温度 | 0.13 mbarで171 °C | ||
| 溶解性 | 930 g・l -l ( 25 °C) | ||
| 密度 | 1.32 g cm -3 ( 47 °C) | ||
| 予防 | |||
| |||
| Rフレーズ: 22、34 、 | |||
| Sフレーズ: 26、36 /37/ 39、45、 | |||
| 生態毒性学 | |||
| DL | 0.89 mg・kg -1 (ラット、経口) | ||
化学式 C 6 H 5 SO 3 H のベンゼンスルホン酸は、ベンゼン環とスルホン酸官能基で構成される有機酸です。これは水中の強酸であり、ベンゼンの芳香族スルホン化によって生成されます。

歴史的
ベンゼンスルホン酸は、1834 年にエイルハルト・ミッチャーリッヒによってベンゼンを硫酸と加熱することによって初めて得られました。これは、1960 年代までアルカリ溶融法によるフェノール製造の主要な試薬の 1 つでした。
使用
ベンゼンスルホン酸は、顔料合成の中間体および酸触媒として使用されます。
物理化学的性質
水とアルコールに非常に溶けやすく、ベンゼンには溶けにくく、ジエチルエーテルや二硫化炭素には溶けません。
三酸化硫黄の存在下でベンゼンと反応して、フリーデルクラフツ反応によりジフェニルスルホニルを形成します。
- $$ {C_6H_5-SO_3H + C_6H_6 \ \Rightarrow[]{SO_3} \ C_6H5-SO_2-C_6H_5 + H_2SO_4} $$
水酸化アルカリと反応すると、対応する金属フェノラートが得られます。
- $$ {C_6H_5-SO_3Na + 2NaOH \ \rightarrow \ C_6H_5ONa + Na_2SO_3 + H_2O} $$
安全
ベンゼンスルホン酸は非常に腐食性の高い生成物であるため、慎重に取り扱う必要があります。加熱すると分解し、有毒な硫黄化合物を生成します。
生産と合成
硫酸を用いたスルホン化により
- $$ {Ar-H + H_2SO_4 \ \rightarrow \ Ar-SO_3H + H_2O} $$
溶媒として、またスルホニル化合物の形成につながる寄生反応を減らすために、約 45% 過剰の硫酸が必要です。
最新の合成プロセスでは、発煙硫酸を介した硫酸の代わりに三酸化硫黄が使用されます。

