原子核は最初は陽子と中性子で構成されています。核物理学では、2 つの原子が同じ数の陽子を持っている場合、その原子は同位体と呼ばれます。原子核内の陽子の数は、原子番号と呼ばれます。 2 つの同位体は同じ原子番号を持ちます。 2 つの同位体を区別するのは、原子質量が異なることです。原子の原子質量は、その原子の核に含まれる核子の数です。したがって、原子量の違いは中性子 N の数の違いによるものです。
評価
同位体は一般に化学記号で指定され、記号の上部と左側に質量数A (原子内の核子の数に等しい) が追加されます。
例: 質量数 14 の炭素 14は14 C と表されます。
同位体が介在する核反応を記述するために、原子番号 Z を記号の左下に配置してこの記述を完了するのが通例です。
炭素14はこうして注目される
したがって、炭素 14

同位体の性質
同じ元素の同位体の化学的性質は、これらの同位体が同じ数の電子を持っているため同一です。
一方、原子核の中性子の数は同じではないため、原子の質量は異なります。この原子量の違いにより、質量分析または遠心分離によって同じ元素の同位体を分離し、区別することが可能になります。さらに、原子核内の中性子の割合によって原子が不安定になる可能性があり、これが原子核が放射性になる理由です。
同位体安定性
自然界には、水素1 H からプルトニウム94 Pu、テクネチウム43 Tc、プロメチウム61 Pm まで、安定同位体も半減期が十分に長い放射性同位体も持たない 92 の異なる化学元素が存在します。
原子核は陽子で構成されており、陽子は電磁相互作用の作用下では互いに反発します(同じ性質の電荷は互いに反発します)が、強い相互作用の作用では互いに引き付け合います。また、強い相互作用の作用下で互いに引き付け合う中性子も含まれていますが、電磁相互作用の影響は(非常にわずかに)受けません。したがって、原子核では、強い相互作用と、ただ存在するだけで陽子を互いに遠ざける中性子によって安定性が確保され、電磁相互作用が減少するため、次のような特性が得られます。
これら何百もの自然同位体の場合、陽子と中性子のそれぞれの数は特定の規則に従っているようです。
- 中性子の数は、軽元素の陽子の数とほぼ同じです。 24 Cr からは、中性子の数が陽子の数よりも多くなり、最も重い元素では過剰が 50% を超えます。
- 特定の特に安定した原子核には、一連の (マジックと呼ばれる) 数の 1 つに等しい陽子または中性子 (あるいはその両方) が含まれています。
- 2、8、20、50、82、126;
これらの値が必要な理由: これらは、中性子または陽子の完全な層を持つ原子核に対応します。完全な層の規則は非常に単純で、電子層の規則と非常に似ています。これらの値を見つけるために、原子核の中心から周縁までの連続した層を考慮します: s1/2 p3/2 1/2 d5/2。 3/2 f7/2 5/2 g9/2 7/2 h11/ 9/2 ルールレベル s には 1+ 1/2.2 の陽子または中性子、または 2 が含まれており、最初の層を構成します レベル p には 1+ 3/2.2+ が含まれます1+1/2.2、つまり 6 をレイヤー s に追加します。つまり 6+2= 8 3 番目のレイヤーにはレベル s と d が含まれています。8 に追加する 10、つまり 20 が簡単に見つかります。4 番目のレイヤーにはレベル p と f が含まれます。つまり 20 ce です。 20+20= 40ですが、原子核の中心によって生成されるポテンシャルは、レベル g の最初の要素が第 4 層に近く、この層に g9/2 または 10 個の核子を追加する必要があることを意味します。したがって、第 4 層が見つかります。 50 核子の場合 5 番目の層には SDG レベル (g 9/2 から切断) が含まれ、h11/2 または 76 を前の 50 に追加すると合計126 になります。たとえば、最も安定な同位体が 82 個の陽子と 126 個の中性子を含む鉛が見つかります。 。それは二重に魔法です。次の値は 184 です。これらは球状のコアです。これらの値の間には、安定性が低い葉巻または皿に変形した原子核が存在します。126 個の陽子を持つ原子核はまだ作成できていないため、間違いなく不安定ですが、2 つの原子を組み合わせることでこの値に近づきます。
- Z 番号が奇数の元素は、Z 番号が偶数の元素よりも安定同位体が少なくなります。
同位体の使用
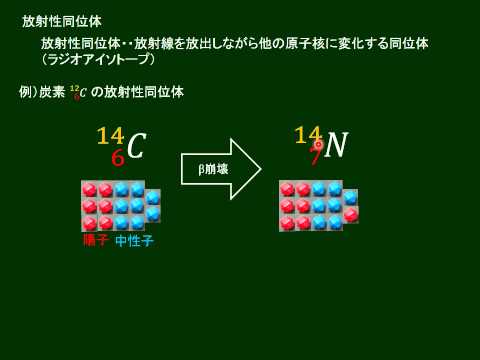
同位体のペアの非常によく知られた例は炭素で構成されます。炭素の大部分は原子量12 の同位体 (「炭素 12」) で存在します。一方、原子量 14 の同位体 (炭素 14) は少量で見つかります。これは化学的に厳密には炭素 12 と同等ですが、放射性です。これは、原子核内の余分な中性子が原子を不安定にするためです。それは崩壊して窒素を与え、ベータ線を放出します。
したがって、不安定同位体に対する安定同位体の割合は時間の経過とともに変化します。同位体ペアを使用する放射性年代測定法は、この変動に基づいています (最もよく知られているのは炭素 14 年代測定法です)。これは確かに同位体概念の最も重要な応用です。同位体トレーサーは、この概念のもう 1 つの応用例です。
主な用途はウランの同位体 235 と 238 の分離で、この分離は UF 6のガス拡散または遠心分離によって行われます。遠心分離モードは、カナダ、ロシア、ヨーロッパの数社のメーカーが担当しています… 遠心分離は、U 235-U 238混合物中の U 235 のレベルを徐々に上げる遠心分離機のカスケードによって行われ、5 分間使用できます。民間核分裂用途の場合は % 濃縮、軍事用途の場合は 90%。遠心分離機は高速で回転する細い円筒です。遠心力はM.w².r に等しいことがわかっています。ここで、M は単位質量、w は回転角速度、r は円柱の半径です。機械的破損を避けるために小さな r を選択し、かなりの力を得るために非常に大きな w を選択します (力は回転の2 乗に比例します)。数千台の遠心分離機を使用すると、望ましい結果が得られます。
他の意味
アニメ『ザ・シンプソンズ』シリーズでは、スプリングフィールドの野球チームはアイソトープスと呼ばれており、そのスポンサーは他でもないスプリングフィールド原子力発電所です。

