ボーア模型は、ラザフォードの惑星模型に基づいた物理理論であり、原子の構成、特に水素および水素化物イオン (電子を 1 つだけ持つイオン) の構成を理解しようとしています。
原理
 |
|---|
このモデルは、水素原子を正に帯電した巨大な原子核として記述し、その周りを負に帯電した電子が移動するアーネスト・ラザフォードの惑星モデルを補完するものです。
このモデルが提起する問題は、古典物理学によれば、加速された電荷である電子がエネルギーを放射し、最終的に原子核に衝突するはずであるということです。
Niels Bohr は、次の 2 つの制約を追加することを提案しています。
- 電子は安定軌道(または静止軌道)にあるときはエネルギーを放射しません。これらの安定軌道は微分され、定量化されます。これらは電子が重力を持つことができる唯一の軌道です。
- 電子は軌道を変えるときにのみエネルギーを放射または吸収します。
したがって、電子の可能な軌道は、量子化された直径の円として記述されます。

理論
水素原子は、陽子を周回する質量mの電子によってモデル化されます。
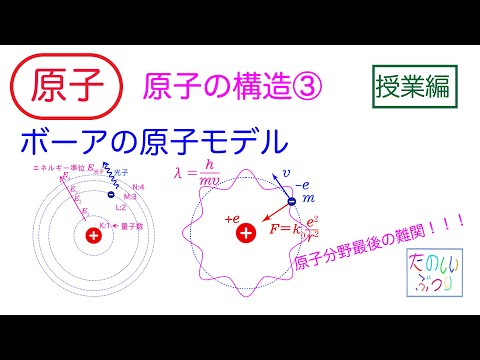
機械エネルギー
これら 2 つの粒子間の相互作用は静電気的であり、介在する力はクーロン力です。したがって、これにより、原子核からの距離rにある電子の位置エネルギーを書くことができます。
$$ {E_p=-\frac{1}{4\pi \epsilon_0}\frac{q_e^2}{r} = -\frac{e^2}{r}} $$
一方、中心力による運動について話しているので、この電子の加速には価値があります。
$$ {\vec{a}= -v^2/r.\vec{u_r}} $$
ここで、 vは電子の速度、 $$ {\vec{u_r}} $$
は遠心単位ベクトルです。したがって、力学の基本原理は次のことを意味します。 $$ {-m\frac{v^2}{r}=-\frac{e^2}{r^2}} $$
次に、運動エネルギーを計算できます。
$$ {E_c=\frac{1}{2}mv^2=\frac{e^2}{2r}} $$
最後に、機械エネルギーを取得します。
$$ {E=E_c+E_p=-\frac{1}{2}\frac{e^2}{r}} $$ |
定量化
ここで角運動量の定量化が始まります
$$ {\vec{L}} $$
ボーアの仮説によれば、次のようになります。 $$ {\ L= n\hbar} $$
ここで、 n はゼロ以外の正の整数であり、 $$ {\hbar} $$
は「換算された」プランク定数です (係数 2 πによる)。この関係は次のように書かれています。
$$ {mrv=n\hbar} $$ |
結果
- 前の 2 つの方程式:
$$ {\frac{mv^2}{r} = \frac{e^2}{r^2}} $$
そして$$ {mvr = n \hbar} $$
原子核と電子の間の距離 r (および速度 v) を計算できます。
$$ {r_n=a_0 \,n^2} $$ |
- または$$ {a_0 = \frac{\hbar^2}{me^2}} $$はボーア半径、およそ午後 53 時です。
- 電子の総エネルギーも定量化されます。
|
と
|
- E 1 はリュードベリ エネルギー (リュードベリ定数を参照) と呼ばれるエネルギーの単位で、約 -13.6 eV に相当します。
- しかし、この理論は、楕円軌道を考慮するためにゾンマーフェルトによって修正されても、1926 年の量子力学革命には耐えられませんでした。
歴史的メモ
- 18世紀から19世紀にかけて、太陽や水素ランプなどのさまざまな光源のスペクトルが分光法によって測定されました。 1750 年の Thomas Melvill (1726-1753) 以来、これらのスペクトルが線によって形成されていることが観察されてきました。
理論分光法は、1859 年に発表されたブンゼン (1811-1899) とキルヒホッフ (1824-1887) の法則によって誕生したと考えられています。ニールス ボーア (1885-1962) は、1913 年にこの定量化現象を初めて説明できました。
- 彼は、水素のスペクトルを構成する線の周波数と2 つのエネルギー項の差を関連付ける式 (バルマーと呼ばれる) の簡単な表現に導かれました。実際、バルマー (1825-1898) は、線の波長を与える次の関係を経験的に発見しました。 $$ {\frac{1}{\lambda} \propto \left( \frac{1}{n^2}-\frac{1}{p^2} \right)} $$これは、オングストロームが可視光線で、ハギンズが紫外線で見つけた線と一致しています。これにより、原子が一定量の定量化されたエネルギー (光子) を放出または吸収するものとして記述することが可能になりました。
- しかし、1911 年のラザフォードの惑星理論は、加速電子放射の理論と衝突しました。実際、この電子はエネルギーを放出し、1ナノ秒に相当する数百万回転後に原子核に衝突することになっていた。
- 1913 年に、ボーアはモデルをこれらの観察と互換性のあるものにするために 2 つの公準を導入しました。電子が原子核の周りの異なる量子化された円軌道を通って移動すると仮定します。電子が軌道を変えると、エネルギーを運ぶ光子が放出されます。したがって、軌道はエネルギー準位になります。以上、水素の原子スペクトルとラザフォードモデルの問題点について説明しました。
- その後、ニールス・ボーアは 1913 年 7 月に論文「原子と分子の構成について」を発表しました。『哲学マガジン』シリーズ 6、第 6 巻。 1913 年 7 月 26 日、1-25 頁。
- その中で、ガイガーの実験 (1913 年) の後、トムソンの原子 (1904 年) ではなくラザフォードの惑星原子 (1911 年) を選んだ理由がよく説明されています。彼は、量子の概念とプランク定数に関してプランクに恩義があることを示しています。彼は、角運動量を考慮するというアイデアを天文学者ニコルソン (1912 年) に与えたと考えています。
いくつかの意見と結果:
- バルマーの公式は、この波長が単色である限りボーアを満たさず、電子のいかなる振動にも対応せず、共鳴がありません。
- 一方、理論上のリュードベリ定数R ∞から 1 個の水素原子R Hのリュードベリ定数への遷移を説明するのに成功したものとして紹介されることが多いにもかかわらず、この記事では還元質量への言及はありません。
- しかし、あまり引用されていないピッカリングの水素の謎は解決されました。天文学者ピッカリングは、n と m を半整数とすること以外はリュードベリの理論に同意する一連の行を発表しました (1895 年)。ファウラーは、水素とヘリウムを入れた管を使った地上実験でこれを確認しました(1912年12月)。次に、ボーアは次の反応のアイデアを思いつきました: H + He → H – + He + 、水素化イオンHe + (リュードベリ定数が 4 倍) のスペクトルが見られ、ピッカリングの水素は存在しないと述べています。 。さらに、彼は有効な整数によるリッツの用語をわずかに変更してアルカリの線を解釈します。
- しかし、彼の理論では、他の原子や分子のスペクトルを解釈することはできません。
- 水素の状態の理論については、1926 年まで待たなければなりません (不確定性原理、飽和を参照)。
