導入
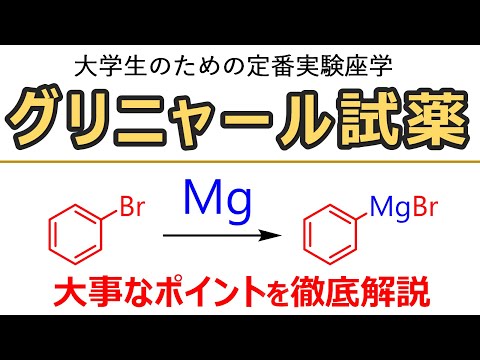
| トリフェニルホスフィン | ||
|---|---|---|
 | ||
| 一般的な | ||
| IUPAC名 | ||
| CAS番号 | 603-35-0 | |
| No.EINECS | 210-036-0 | |
| 笑顔 | ||
| インチチ | ||
| 外観 | 臭いのない白色の結晶。 | |
| 化学的性質 | ||
| 生のフォーミュラ | C午後6時15分 | |
| モル質量 | 262.2855 ± 0.0155 g・mol -1 | |
| 物理的性質 | ||
| 融解温度 | 80 ℃ | |
| 沸騰温度 | 377 ℃ | |
| 溶解性 | 水中:ゼロ | |
| 密度 | 1.1g・cm -3 | |
| 引火点 | 180 ℃ (オープンカップ) | |
| 熱化学 | ||
| CP | ||
| 予防 | ||
| ||
| Rフレーズ: 22、43、53 、 | ||
| Sフレーズ: 24、37、61 、 | ||
1 0 0 | ||
| 生態毒性学 | ||
| DL | 700 mg・kg -1 (ラット、経口) | |
| 露出値 | 5mg・m -3 | |
トリフェニルホスフィン(またはトリフェニルホスファン) は、式 P(C 6 H 5 ) 3 (PPh 3または Ph 3 P と略されることもあります) を持つ有機リン化合物です。有機および有機金属化合物の合成に広く使用されています。これは比較的安定した化合物で、室温では結晶固体として存在し、ベンゼンなどの非極性溶媒に溶解します。

準備
トリフェニルホスフィンは安価ですが、三塩化リンを臭化フェニルマグネシウムまたはフェニルリチウムで処理することにより実験室で製造できます。工業的な合成には、三塩化リンとベンゼンの間のフリーデルクラフツ反応が含まれます。トリフェニルホスフィンは、熱エタノールまたは熱イソプロパノールから再結晶できます。この精製は、空気によるゆっくりとした酸化によって形成される式 OP(C 6 H 5 ) 3のトリフェニルホスフィンオキシドを除去するために推奨される場合があります。
無機化合物および有機金属との反応
トリフェニルホスフィンは、配位錯体を形成するための金属カチオンの配位子としてよく使用されます。ほとんどの遷移金属、特にパラジウム、白金、ルテニウム、ニッケル、オスミウムなどの中期から後期のdブロック金属に結合します。例: パラジウム(0) テトラキス(トリフェニルホスフィン) 。対応するトリフェニルアミンは遷移金属に対して低い親和性を持っています。この違いは、窒素原子のサイズが小さいことで説明され、その結果、立体遺伝子が大きくなり、金属中心へのリガンドの接近が制限されます。
金属-P(C 6 H 5 ) 3タイプの化合物は31 P NMR 分光法によって特徴付けられます。
トリフェニルホスフィンは、元素硫黄を含む多くの硫黄化合物から硫黄を捕捉します。リン生成物は SP(C 6 H 5 ) 3です。この反応は硫黄レベルの分析に使用できます。
主な有機反応
P(C 6 H 5 ) 3 は有機合成で広く使用されています。 P(C 6 H 5 ) 3とハロゲノアルカンの反応により、ホスホニウム塩とも呼ばれるリン酸塩が生成します。
これらの塩は強塩基(有機金属タイプ、たとえば有機リチウム、アミドイオン -NH 2 –または水素化物H – 、場合によってはそれほど強力ではない塩基も使用できます)と反応して、ホスホランとも呼ばれるリンイリドを形成します。
これらの分子は特にウィッティヒ反応で使用され、その場で生成され、カルボニル化合物、アルデヒド、またはケトンと反応してエチレン誘導体、さらにはアルケンを形成します。
P(C 6 H 5 ) 3と塩素の反応により Cl 2 P(C 6 H 5 ) 3 が生成され、その場で生成されてアルコールが塩素化誘導体に変換され、同時にHClとトリフェニルホスフィンオキシド O= P( C6H5 ) 3 .