相図は熱力学で使用される式です ( 「相」を参照)。これは、理解を容易にするために選択された変数の関数として、システム (純粋な物体または純粋な物の混合物) の物理的状態 (または位相[ 1 ] ) の領域を表す、一般に 2 次元または 3 次元のグラフィック表現を示します。研究された現象の。
最も単純な図は、温度と圧力を変数とする純粋な物体に関するものです。よく使用される他の変数は、エンタルピー、エントロピー、質量体積、および混合物を構成する純粋な物質の 1 つの質量または体積の濃度です。
研究対象の系がn 個の純粋な物体の混合物である場合、その物理的状態は、その成分の(n-1)個の独立した比率、および温度と圧力によって定義されます。したがって、2 変数ダイアグラムは、システムの(n-1)個の変数を固定することによってのみ確立できます。
これは、通常の大気圧(過冷却) で 0 °C 以下の温度の液体の水など、準安定状態にある系を記述することを可能にしない平衡図です。
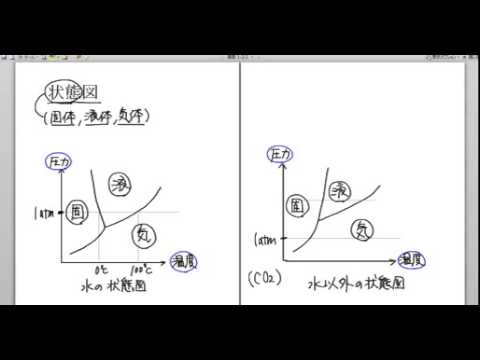
純粋な体の状態図
純粋な物体は、圧力と温度の条件に応じて、固体、液体、気体の 1 つまたは複数の相で存在します[ 2 ] 。一般に、純粋な物体は、次の場合を除き、特定の圧力と温度において単一相で存在します。
- 三重点では、3 相が所定の温度と圧力で共存します。
- 状態の変化(または相転移)に対応する対(圧力、温度)の場合、次のいずれかになります。
表現されたすべてのフェーズが異なる物理状態に対応する場合、状態変化図について話すことがあります。
一般に、図では状態変化曲線が増加しています。
純粋な体相図の例
水相図
大気と接触した純粋な物体は、純粋な物体を含む系を構成しないことに注意する必要があり、これは、例えば、水が通常、室温で液体状態と蒸気状態で共存することを説明する。沸点(常圧で100℃)から。
固体状態では、圧力と温度の範囲に応じて、物体はいくつかの結晶化形態をとることがあります。したがって、結晶化の各形態は異なる相を構成し、それによって状態図を描くことが可能になります。
いくつかの結晶化形態の状態図の例: 氷 — 前の図と比較すると、軸が逆になり、圧力スケールは対数になっています。
二元図と三元図
2 つの純粋な物体で構成されるシステムがある場合、そのシステムはいくつかの形式をとることができます。
- 完全に固体であり、それぞれの物体は別々に結晶化します。
- 完全に固体であり、2 つの物体は固溶体または特定の化合物の形で完全に混合されており、加熱により分解する方法に応じて共晶、共析、包晶または包晶と呼ばれます。
- 固液混合物。
- 完全に液体、2 つの混ざらない液体 (エマルション)、または単一の完全に均質な液体 (単相、溶液) の形態。
- 液体と気体の混合物(エアロゾル、または液体上の気体)。
- ガス(ガスは高度がわずかに変化しても常に均一です)。
上記の状態は、単一相 (混和性の液体または気体など) またはいくつかの不均一相のいずれかで構成されます。同様に、システムの状態を圧力、温度、組成の関数としてプロットすることができます。
n 個の純粋な物体の場合、 n 個の濃度がありますが、圧力と温度に関する独立したパラメータはn+1個だけです。実際、濃度の合計は 100% に相当し、濃度の 1 つは他の濃度から推定できるため、独立したパラメーターを構成しません。
したがって、これらのn+1 個の独立したパラメーターを表すには、 n+1次元の図が必要になります (2 つの純粋な物体については 3 次元、3 つの純粋な物体については 4 次元)。表現を簡素化するために、2 次元図を描くために十分な数のパラメータが固定されています。私たちはよく次のような図を検討します。
- 特定の組成について、純粋な物体図にあるものと同様の圧力-温度状態図 ( P 、 T )。
- 特定の圧力と 2 つの純粋な物体の場合、二成分組成温度図 ( c , T )。
二元図の例: 大気中の水と塩の図
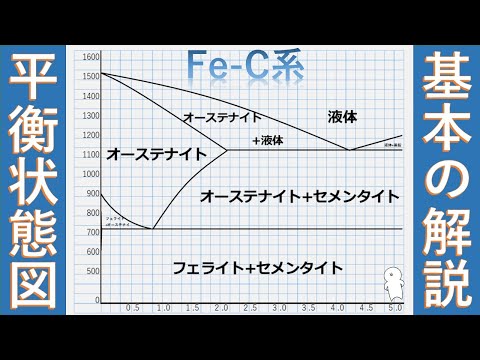
二元図の例: 大気中の鉄-炭素図
- 与えられた圧力と温度、および 3 つの純粋な物体の場合、三元ダイアグラム ( c 1 、 c 2 )、つまり組成の関数としての位相。習慣により、 c 3 = 1- c 1 – c 2ですが、この図を正三角形( c 1 , c 2 , c 3 ) で描きます。
単一固溶体図
銀と金の合金など、化合物が定義されていない場合もあります。このような場合、バイナリ図は以下に示すように非常に単純になります。
我々は持っています
- T 純粋な物体Aの融解温度で;
- T B純粋な物体Bの融解温度。
以下を定義します。
- 液相線: この曲線より上では、生成物は完全に液体です (これが上部の曲線です)。液相線は、特定の温度で固体と平衡にある液体の組成を定義します。
- 固相線: この曲線の下では、生成物全体が固体です。固相線は、特定の温度で液体と平衡にある固体の組成を定義します。
液相線と固相線の間には、固体と液体の混合物が存在します。この図により、凝固がどのように起こるかを予測できます (この記事を参照)。
定義された化合物
定義された化合物は、一定温度で相変化が起こる化合物です。私たちは以下を区別します。
- 共晶: 共晶は一定の温度で溶け、実際には純粋な物体のように振る舞います。
- 共析: 共析は一定温度で固相変態を起こします。共晶との唯一の違いは、温度限界を超えた相は液体ではないことです。
- 包晶: 一定温度で固体 A →固体 B +液体の変態が起こります。
- 包晶質: 一定温度で固体 A →固体 B +固体 Cの変態が起こります。
ダイアグラム(P、V、T)
純粋な物体の状態変化 (気体、液体、固体) の場合、結果は 3 次元図の形式で表される場合があります。軸は圧力P 、システムが占める体積Vおよび温度です。 T.
古典的な純粋体の図 (P、V、T)
水の図 (P、V、T)
この 3 次元図は、実際には、熱力学で使用される 3 種類の図 (状態変化図、クラペイロン等温図、等圧図) から構成されています。
以下の図は、熱力学図を図 ( P 、 V 、 T ) の「切断」または「投影」として示しています。矢印は投影の方向を示します。
純粋な物体の状態変化の図 ( P 、 V 、 T ) および図 ( T 、 P )
ダイアグラム ( P 、 V 、 T ) およびクラペイロン等温線図
ダイアグラム ( P 、 V 、 T ) と等圧ダイアグラム ( V 、 T )
相図はどのように作成するのですか?
状態図は実験的に確立されます。つまり、条件が変化し、相変化が観察されます。
位相変化はいくつかの方法で観察できます。
- 熱を生成するもの (例:凝縮または発熱化学反応)、または熱を吸収するもの (例: 融解または吸熱化学反応) があるため、熱流を測定することで、相変化が起こっているかどうかを知ることができます。これは熱示差分析 (TDA) です。
- 体積の変化、収縮(固体の原子の凝縮またはよりコンパクトな配置への再配置など)、または膨張(固体の原子の蒸発またはそれほどコンパクトでない配置への再配置など)の変化を引き起こすものもありますが、その場合は次のようにするだけで十分です。たとえば可動ピストンを使用して、質量の重量または油圧システムによって加えられる力の体積変化を測定します。
- 逆に、圧力計を使用して、エンドレススクリューによって作動する可動ピストンを体積に加えることで、圧力の変化を観察することができます。
- 系の状態を肉眼で観察します(結晶の融合など)。
- 異なる固相の場合、異なる結晶相は X 線回折によって認識できます。熱いサンプルで分析を実行したり、サンプルを浸したりすることもできます。つまり、サンプルが冷たいときでも平衡構造を熱い状態に保つように急速冷却します(したがって平衡状態ではありません)。
圧力をかけることで体積の変化を測定できる実験装置
状態温度の変化を決定するために使用される凝固曲線は、単純化された熱微分分析から得られます。液体を冷却し、その温度を測定することから成ります。熱損失率はシステムと外部の温度差に比例するため、指数関数的な曲線が得られます。プラトーが観察される場合、それはサンプルが凝固の特徴である熱を放出していることを意味します。固体の相変化(結晶構造の変化)中に、同様にプラトーを観察できます。
凝固曲線、等圧、受動的冷却、純粋な本体または共晶合金の場合
注意事項
- ↑物理学では、特定の状態 (気体、液体、非晶質固体、何らかの形で結晶化した固体) にある純粋な物体、または純粋な物の均一な混合物を相 と呼びます。
- ↑高温では、純粋な物体がプラズマの形で現れ、物質の 4 番目の状態と考えられます。
- ↑臨界温度を超える温度、または臨界圧力を超える圧力。
- ↑温度が臨界温度よりも高い気体は超臨界と呼ばれます。圧縮だけで液化することは不可能です。