理想気体は、低圧pにおけるすべての実在気体の挙動を記述する熱力学モデルです。
このモデルは、ガスの化学的性質が何であれ、十分に低い圧力ではすべてのガスが同じ挙動を示す傾向があることを観察することによって19世紀に開発されました。これは 1811 年に発見されたアボガドロの法則、つまり圧力、体積、圧力の関係によって表されます。これらの条件下では、温度はガスの性質に依存しません。これは非常に異常に思えたので、信じるのに時間がかかりました (アボガドロの数の記事を参照)。この特性は、圧力が低い場合、ガスの物理化学的性質 (多かれ少なかれ極性のある分子) に依存する静電相互作用を無視できるほど、ガス粒子が互いに十分に離れているという事実によって説明されます。多くの実際の気体は、通常の条件下では、優れた近似で理想気体モデルを満たします。これは、空気、窒素、二酸素などの主なガスの場合に当てはまります。
理想気体の説明
巨視的な面では、理想気体とは、ボイル・マリオットの法則とアボガドロの法則を同時に満たす気体です。
- ボイル・マリオットの法則
- 一定の温度では、圧力pと体積Vの積: pV は、圧力が低いときは一定とみなされます。
- アボガドロの法則
- 同じ圧力と温度の条件下では、すべてのガスは同じモル体積を持ちます。
微視的なレベルでは、 気体の運動理論により、この理想気体の挙動を見つけることができます。理想気体とは、その分子が衝撃以外では相互作用せず、そのサイズが分子間距離の平均に比べて無視できる気体です。したがって、理想気体のエネルギーは、分子の質量中心の運動エネルギーと各分子の内部エネルギー(回転、振動)の和になります。これら 2 つのエネルギーが比例すると、完全なラプラス気体が得られます。
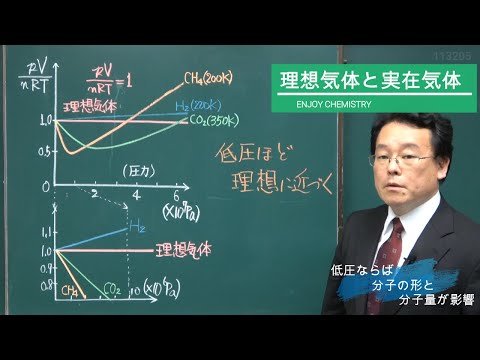
モデルの制限と実際のガス
低圧では、すべての気体は理想気体としてモデル化できます。圧力が増加すると、短距離相互作用、特に分子のサイズ効果やファンデルワールス型相互作用を無視できなくなります。
風刺的に言えば、圧力をさらに高めると気体は液化します。当然のことながら、液体は理想気体とは言えません…
分子間距離が分子のサイズや相互作用力の範囲に比べて大きい場合、現実の気体は理想気体に近い挙動をします。一定圧力における熱容量がゼロ圧力における実在ガスの熱容量C p ( p = 0, T )である理想気体を「実在ガスに関連する」理想気体と呼びます。この関連する理想気体に加えられた補正から、現実気体の熱力学表を作成します。
状態方程式とジュールの法則
あらゆる気体と同様に、理想気体の熱力学的平衡状態は、選択した 2 つの巨視的パラメータによってnモルの分子に対して固定されます。他のパラメータは、「状態方程式」と呼ばれる公式によって選択された 2 つのパラメータから計算できます。
最も一般的に使用される方程式は、熱弾性方程式である理想気体方程式です。これは 2 つの形式で記述することができます。1 つは巨視的 (気体の体積Vを含む) であり、もう 1 つは体積単位に含まれる分子の数を考慮する、より微視的なアプローチです。
- $$ {pV = nRT\ ou\ pV = Nk_BT=nN_Ak_BT~} $$
または
- p は圧力 (パスカル) です。
- Vはガスが占める体積 (立方メートル);
- nは物質の量(モル単位)
- N は粒子の数です
- R は理想気体定数です
R = 8.314 472 J K -1モル-1
実際にはR = N A · k Bになります。ここで、 NAはアボガドロ数 (6.022×10 23 )、 k B はボルツマン定数(1.38×10 -23 ) です。 - T は絶対温度(ケルビン単位) です。
この方程式は実際には、以前に発見された他の法則、つまりシャルルの法則、ボイル・マリオットの法則、ゲイ・リュサックの法則から派生しています。
デジタルアプリケーション:
- 1気圧の場合 ( p = p 0 = 1.013 25×10 5 Pa)
- 温度が 0°C ( T = T 0 = 273.15 K、 p 0で氷が溶ける温度)、
したがって、モル体積は
- V 0 = 22.413 996(39) L/mol
通常、およその値 22.4 L/mol を維持します。
これは、分子あたりの体積 (サイズとは関係なく、分子周囲の「自由」体積) を示します。
- $$ {\frac{V_0}{N}} $$
この自由体積を立方体に同化すると、この立方体の端は、各瞬間における分子を隔てる全体的な平均距離となり、これをロシュミット長d 0と呼びます。この値は、「空き」ボリュームの立方根です。
- d 0 = 3.338 792 5 nm
通常は、およその値 3.33 nm を使用します。
大気圧の 100 万分の 1 に相当する圧力 ( p 0 /1,000,000) の場合、粒子間距離は 333 nm = 1/3マイクロメートルであり、ガスの性質には依存しません。
エネルギー方程式、ジュール・トムソンの法則を使用することもできます。
- エンタルピーH ( p , T ) = U + p 。 Vは圧力に依存しません。
これら2 つの定義式から、内部エネルギーU ( V , T ) は体積ではなく温度のみに依存することがすぐにわかります。理想気体はジュールの法則に従います。
理想気体の一定体積における熱容量は次のようになります。
- $$ {C_V = N \left( \frac { \partial U}{ \partial T}\ \right)_V} $$
したがって、ボリュームとは独立しています。
同様に、理想気体の定圧における熱容量は次のようになります。
- $$ {C_p = N \left( \frac { \partial H}{\partial T}\ \right)_p} $$
したがって、圧力の影響を受けません。
定義上、エンタルピーには価値がある
- $$ {H = U + pV~} $$
Mayer 関係式が得られます。
- $$ {C_p – C_V = R~} $$
1モルあたり。
膨張の潜熱伝達の膨張潜熱l を与えるクラペイロンの公式を適用すると (熱力学的公式を参照)、等容圧の相対増加の係数β が次を満たすことがわかります。
- $$ {\beta T = 1~} $$、
それで :
- U(V,T) は体積に依存しません。理想気体はジュール気体です。 $$ {U = N\cdot u(T) +cste~} $$
そしてエンタルピーは次のとおりです。
- $$ {H(p,T) = U + pV~} $$
したがって、 はpに依存しません。理想気体はジュール-トムソン気体です (ジュールの法則を参照)。
ラプラス完全ガス

意味
それは起こります
慣例により、私たちが選択する場合
慣例により、私たちが選択する場合
理想的なラプラス気体については、次のように書くのが通例です。
- $$ {pV =( \gamma -1) \cdot U = (1- \frac{1}{\gamma}) \cdot H} $$
つまり、単原子理想気体の場合
- pV = 2/3 U = 2/5 H
二原子理想気体の場合:
- pV = 2/5 U = 2/7 H。
ラプラスの法則
基本的な可逆断熱変換では、次のようになります。
- $$ {dU = – p.dV \,} $$
U をpとVの関数としての値に置き換えると、次の結果が得られます。
- $$ {V.dp + \gamma.p.dV = 0~} $$
以下を統合することによって:
したがって、これらのやや珍しい理想気体に付けられた名前です。
この結果、膨張し、かなりの冷却が起こり、ガスは内部エネルギーとして仕事 (- W ) を受け取り、それが提供されます。
( 「断熱膨張」も参照)。
数値的応用: 単原子理想気体の場合、次のことが簡単にわかります。
- $$ {\ln \frac{T}{T^0} = \frac{2}{5} \cdot \ln \frac{p}{p^0}} $$
圧力比 1/10 (圧力が 90% 低下) の場合、絶対温度は 0.398 分の 1 に減少します。温度は 300 K から 120 K まで下がり、180 K も下がります。このプロセスは、低温を得るために産業界で使用されています。残念ながら、実際の気体は低温では理想気体ではないため、得られた値は少し理想的です。
桁違いの場合は、
- R・T ~ 2500 J/mol (300 K)。
したがって、このリラクゼーションで回復される作業は次のとおりです。
- 2500・(180/300) = 900 J/mol。
実験:空の容器でリラックス
もう 1 つの注目すべき法則は、ラプラス理想気体が空のフラスコに浸透するときに生じる発熱です。ガスが勢いよく流れ込み、すぐにすべてが再び混沌となります。温度は均一になり、
- T = γ T 0
T 0は外部温度です。外部温度 300 K および単原子理想気体の場合、次の式が得られます。
- T = 500K
つまり、標高 200 K です。Modane 風洞では、これが観察できます。
したがって、ガス膨張の 2 つのケースがあります。 2 つ目は、これまで考えたことがない人にとっては少し驚くべきことです。
( 「断熱圧縮」の記事も参照してください。)
理想ラプラス気体のカルノーサイクル
カルノーの定理が示すように、理想気体を駆動するカルノー サイクルのカルノー効率は次のようになります。
この場合、すべてを簡単に計算できます。サイクルを説明しましょう。対数クラペイロン座標 (log V 、 log p ) で簡単に描くことができます。
- 変態 (A → B): 低温T 2での等温圧縮、可逆的: したがって、ガスの加熱を防ぐために、温度を維持する低温源に熱量– Q 2 > 0 を放出する必要があります。 T2 。
- 変換 (B → C): ラプラス圧縮: 温度はT 2からT 1に上昇します。
- 変態 (C → D): 高温T 1での等温膨張、可逆: ガスの冷却を防ぐために、高温源はQ 1 >0 の熱量を提供する必要があります。
- 変換 (C → A) (点C は、A を通過する可逆断熱の交点で選択されました): 可逆断熱膨張により、温度がT 1からT 2に低下し、気体が初期状態に戻ります。
サイクルの終わり。
気体は初期状態に戻っているので、熱力学の第一法則から次のことが分かります。
- W + Q1 + Q2 = 0
モーターの効率は、回収される仕事 – W (したがってQ 1 + Q 2に等しい) を高温源、つまりQ 1によって供給される熱量で割ったものです。
- $$ {r = 1 + \frac{Q_2}{Q_1}} $$
私たちはそれを実証します
- $$ {\frac{Q_1}{T_1}+\frac{Q_2}{T_2} =0} $$
したがって
- $$ {r = -\frac{W}{Q_1}= 1-\frac{T_2}{T_1}} $$。
これにより、発表された公式が得られます。
クラウジウスの平等
- $$ {\frac{Q_1}{T_1} + \frac{Q_2}{T_2} = 0} $$
これは、サイクルが可逆的であったという事実に由来しています。つまり、総エントロピーは一定のままで、状態 A に戻ったためガスのエントロピーはゼロです。ソース 1 では、そのエントロピーが – Q 1 / T 1だけ変化することがわかり、ソース 2 では – Q 2が変化しました。 / T 2 、したがって等価です。
数値的応用:300Kの川の水と600Kの温泉を採取したとしても、収率は50%に過ぎません。 「可逆的」発電所によって供給されるギガワットの電力では、2GW が (石炭、石油、メタン、または核燃料ガスとして) 消費されなければならず、そのうち 1GW は川 (温度の上昇) または大気中 (煙) に流れ込みます。熱、冷却塔からの蒸気)。すべての熱が川に流れ込み、川の流量が100 m 3 /s であると考えると、1秒間に、10 9 J は 100×10 6 g の水を加熱します。つまり、温度が 10 ( J)/4.18 (J/K) = 2.4 K。
6 GW を生産する 6 つの発電所の標高は、6・2.4 = 14.4 K になります。 フランスでは、川で 27°C を超えることは禁止されています (温帯の水生生物の生存のための法的義務)。 2003 年は非常に暑く、いくつかの発電所は停止しなければなりませんでした (記事「Heatwave 2003 」を参照)。カルノーの公式によって計算されるこの熱汚染( Q 2 < 0) は可能な限り低くなります。これは実際には最小限であり、実際の熱汚染はさらに高くなります。ここでも収率r = 0.5 をとりました。実際は 0.42 に近いです。
ジュールの実験
これが 3 番目の例です。今回は、理想気体が体積V 1のボトルに含まれており、突然体積V 2の空の容器と接触し、そこで部分的に飲み込まれます。壁が完全に閉じられていると仮定すると、最終温度は何度になりますか?熱を吸収しないのですか?
この体験は、ジュール&ゲイ・リュサック体験、またはジュール リラクゼーションとさえ呼ばれます。実際、それを実験的に実装することに実際に成功したのは 1856 年の Hirn でした。
何が起こっているのか少し疑問があります。2 番目のコンテナではガスがもっと熱いはずです。 V 2 がV 1よりもはるかに低い場合、実験 2 に従ってT 2 = γ · T 0を見つける必要があります。
コンテナ 1 では、そこに残っているガスが膨張しており、より低温になっているはずです。これが私たちが見ているものです。しかし、熱平衡に戻った後の最終的な温度は何度でしょうか?答え: GP はジュール気体であるため、温度は変化しません (ジュールの法則を参照)。

理想気体のエントロピー
気体についてすべてを知るために残っているのは、そのエントロピー S を計算することだけです。 T (絶対温度) が熱力学温度 (温度測定) であるという事実を認めれば、これは簡単です。
それで書いています
- $$ {dS = \frac{1}{T} \cdot (dH – V \cdot dp) = C_p \cdot \frac{dT}{T} – R\cdot \frac{dp}{p}} $$
それはすぐに来ます:
- $$ {S(p,T) = S_{\rm molaire} = C_p \cdot \ln T – R \cdot \ln p + {\rm constante}} $$。
例: 前のジュール実験では、不可逆的かつ断熱的で、エントロピーが増加しました。
- $$ {\Delta S = R \cdot \ln \left (1 + \frac{V_2}{V_1} \right )} $$。
統計力学(量子) のみが、いわゆるサッカー四極管定数の値を与えることができます (熱力学の第 3 法則を参照)。
単原子理想気体の場合、次の値を保持することを好みます。
- $$ {G = U + p \cdot V – T \cdot S} $$
自由エンタルピーと呼ばれます:
- $$ {G(V,T,N) = – N \cdot k \cdot T \ln \frac{p}{p^0}} $$
と
- $$ {p^0(T) = \frac{kT}{\lambda^3}} $$
または
- λ はドブロイ波長です$$ {\lambda = \frac{h}{p}} $$
- h はプランク定数です
- pは運動量です$$ {p = \sqrt{2 \pi \cdot m \cdot k \cdot T}} $$
次に、表に示されているすべての値を見つけます (たとえば、アルゴン、ネオンなど)。二原子気体の場合、計算はほとんど複雑ではありません。
この値は、原子間距離がド ブロイ波長よりもはるかに大きい場合にのみ有効です。
- $$ {d = \sqrt(lien){V/N} width=} $$> \ラムダ” >
それ以外の場合、私たちは冷たい原子ガスの領域に陥ります(超低温原子の研究は、クロード・コーエン=タンヌージのノーベル物理学賞の対象でもあります)。
理想気体と気体の運動理論
理想気体は、気体の運動理論と呼ばれる理論の主題であり、それを支配する物理法則を説明します。
理想気体の混合物
理想気体の理想的な混合物については、ダルトンの法則があります。
p = ∑ ぴー 私
ここで、 p i は、気体iの分圧、つまり、気体iが単独で全体積を占める場合の圧力を示します。
体積V 1を占める分子Aの理想気体と体積V 2の分子Bの理想気体を考えてみましょう。隔壁によって分離されており、それらは平衡状態にあります (同じ温度Tおよび同じ圧力P 0 )。同じ圧力および同じ温度では、隔壁を除去することによって得られる混合物が同じ圧力、同じ温度および体積V 1 + V 2の系であることはまったく明らかではありません。比較のために、1 L の水と 1 L のアルコールを混合すると、1.84 L のアルコール水が得られます。確かにそれらは理想気体ではありませんが、これは特性が必ずしも相加的であるわけではないことを示しています。
ガスが化学的に中性である、つまりAとBの分子が相互作用しないと考えてみましょう。前の段落によれば、
- 次に、 A はB を「見ていない」(相互作用がない) ため、 V 1からV 1 + V 2へのジュール膨張を受けます。
- 対称的に、 B はV 2からV 1 + V 2までジュール膨張します。
したがって、温度は変化しておらず、壁にかかる圧力はAとBによるものです。
- $$ {p_A = p_0 \left ( \frac{V_1}{V_1+V_2} \right )} $$Aの貢献に対して、そして
- $$ {p_B = p_0 \left ( \frac{V_2}{V_1+V_2} \right )} $$B さんの貢献に感謝します。
全圧力はp A + p B = p 0です。圧力は変化していないため、マリオットの法則は真実のままです。一方で、「混合による情報の損失」(ギブスのパラドックス)がありました。
AとBの間に相互作用がない場合、内部エネルギーは単にAのエネルギーにBのエネルギーを加えたものになります。つまり、ジュールの法則は真実のままです。したがって、混合物は理想気体のように振る舞います。
2 つのラプラス理想気体の混合物はラプラス理想気体ですが、その係数 γ は γ の加重平均ではなく、加重平均であるC VとC pです。
混合物のエントロピーは、その分圧下で取得された各ガスのエントロピーの合計です (ギブスのパラドックスを参照)。この点は非常に重要です。これは化学における集団作用の法則の鍵となります。
